Antimikrobiyal direnç
Antimikrobiyal direnç büyük bir küresel sağlık riski oluşturmaktadır. Bir zamanlar tedavi edilmesi basit olan enfeksiyonlar, bakteriler daha önce etkili ilaçlara karşı direnç geliştirdikçe hayatı tehdit edebilir. Bu zorluk sadece yaygın hastalıkları değil, aynı zamanda ameliyatlar ve kanser tedavileri gibi kritik tıbbi prosedürleri de etkiler.
Artan direnç oranları, sınırlı etkinliklerine rağmen son resort tedavileri olarak polimiksinler gibi eski antibiyotiklere güvenmeyi zorlamıştır. Bu bağımlılık özellikle alternatiflerin az olduğu düşük gelirli ortamlarda belirgindir.
Polimiksinler bakterileri nasıl öldürür?
80 yıl önce keşfedilen polimiksinler, gram negatif bakterilerin neden olduğu enfeksiyonları tedavi etmek için kullanılır Escherichia coli. Bu tür bakteriler, birçok antibiyotiğin hücreye girmesini engellemeye yardımcı olan bir dış zar içerir. Bu dış zarın ana bileşenleri lipopolisakkaritler (LPS) ve dış membran porinler (OMP'ler). Polimiksinlerin bu koruyucu katmana saldırdığı bilinse de, onu bozdukları ve bakterileri başarıyla öldürmenin kesin yolu belirsizliğini koruyor.
Alandaki yaygın bir yanlış anlama, membran hedefleme antimikrobiyallerinin hareketsiz bakterilere karşı etkili olmasıdır. Uykuda bakteriler, büyümeyi ve bölmeyi bıraktıkları ancak hala hayatta oldukları geçici bir aktif olmayan duruma giren bakterilerdir. Bu, çevre daha uygun olduğunda zorlu koşullardan kurtulmalarını ve “uyanmasını” sağlar. Membran esasen bakterilerin aktif veya uykuda olduğu için aynı olduğundan, hipotez, polimiksinlerin aktivitelerinden bağımsız olarak onu hedefleyebileceğidir.
Ama bu gerçekten polimiksinler için geçerli mi? Aslında uykuda bakterileri öldürüyorlar mı?
Yöntemlerimiz
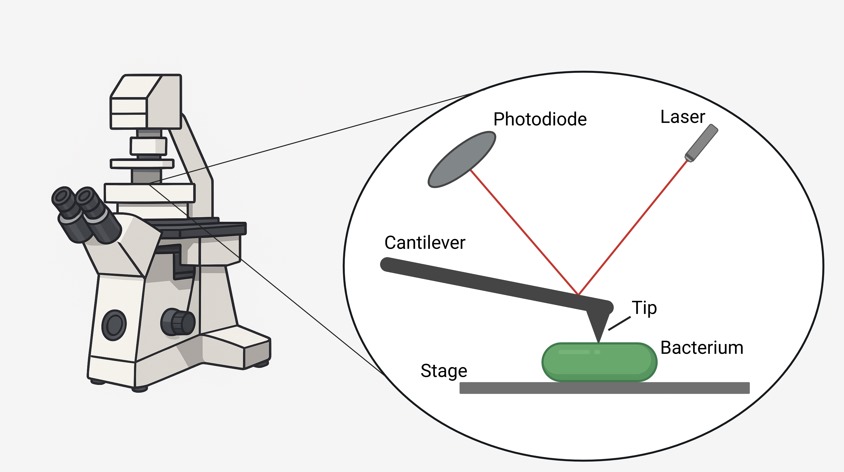
Atomik kuvvet mikroskopisi (AFM) dahil olmak üzere biyokimyasal ve biyofiziksel yöntemlerin bir karışımı kullanarak, polimiksin B (PMB) uykuda ve aktif bakterilerde moleküler düzeyde nasıl davrandığını araştırdık. AFM, bir numunenin (yani bakteriler) yüzeyini hafifçe tarayan ve örnek topografinin yüksek çözünürlüklü bir görüntüsünü oluşturan inanılmaz derecede keskin bir uçtan yararlanır. Bu, mikrobiyolojide nispeten yeni bir araçtır ve grubumuz bunu doğrudan canlı bakteriyel hücrelere uygulayan ilk kişiler arasındadır. Bu yaklaşımı tam olarak kullanmak için işbirliğimiz, önde gelen üç üniversitede uzmanlığı bir araya getiriyor – Imperial College London, UCL ve Nottingham Üniversitesi.
Polimiksinler zarını büyük ölçüde bozuyor E. coli
Bu soruyu cevaplamaya çalışırken gözlemlediğimiz ilk şey E. coli Uygun koşullarda, yani besinlerin varlığı. Bu etki, gerçek zamanlı olarak tedavi gören bakterilerin AFM görüntülerinde görüldü: aksi takdirde pürüzsüz dış zar hızla çıkıntılar ve genel düzensizlik ile dolu oldu. AFM ile antibiyotiğin etkisini 90 dakikadan fazla gerçek zamanlı olarak izleyebildik. PMB'nin bu dış zarda ne kadar hızlı bir şekilde bozulmaya neden olduğunu ve nihayetinde ölmeden önce bakterilerin ne kadar hasar verebileceğini görmenin büyüleyici olduğunu gördük. Sadece bu değil, aynı zamanda bir dizi mikrobiyolojik ve biyokimyasal analizle, dış zardaki LP'lerin çoğunun bakterilerden salındığını kanıtladık. Hücre PMB'nin kendisine bağlanmasını algılıyor gibi görünüyor ve tedavi sonucunda daha fazla dış membran üretmeye zorlanıyor, o kadar hızlı bir şekilde dengesizleşiyor ve antibiyotiğin girmesine izin veren açıklıklar yaratıyor.

Polimiksinler metabolik olarak inaktif bakterileri öldüremez
Bununla birlikte, glikoz gibi besin maddelerinin yokluğunda hareketsiz bakterileri PMB ile tedavi ederken, bu dış zar sağlam kaldı ve ondan LP'lerin dökülmesi yoktu, bu antibiyotik sınıfının uykuda olan bakterilere karşı etkisiz olduğuna inanmamıza neden oldu. Mikrobiyolojik deneyler aracılığıyla, PMB'nin hala dış zarı bağlayabildiğini, ancak ona nüfuz edemediğini ve bu hareketsiz hücreleri öldüremediğini gözlemledik.
İşbirliğimiz
Araştırma boyunca, kurumlar arasındaki işbirliği, bu çalışmayı gerçekten bu kadar etkili hale getirdiğine ve bu çalışmada elde edilen hızlı ilerlemeye izin verdiğine inandığımız şeydir. Bu işbirliğinin disiplinlerarası doğası, her biri cevaba benzersiz ve değerli bir şey getiren aynı soruyu birden fazla açıdan incelememizi sağladı. Örneğin, çeşitli tedavi koşulları başlangıçta mikrobiyolojik deneyler kullanılarak değerlendirildi (örneğin, zaman öldürme deneyleri). Bu koşullar daha sonra doğrudan karşılaştırmaya izin vermek için AFM veya taranan elektron mikroskobu (SEM) deneylerinde çoğaltıldı. Mikroskopide, genellikle bir seferde bir veya iki hücreye bakarız, özellikle bir tedavinin etkilerini izlerken, bu nedenle tek hücreli düzeyde olanları popülasyon seviyesiyle ilişkilendirebildik.
Bu çalışma, polimiksinlerin bakterileri nasıl öldürdüğüne dair yeni bir model öneriyor. Önce dış zarına bağlanırlar E. coli, hücrelerin metabolik olarak aktif olup olmadığına bakılmaksızın. Daha sonra, aktif hücrelerde, bu yeni LP'lerin sentezine ve taşınmasına bağlı olan LPS salınımı ile sonuçlanır. Bu da, polimiksinlerin iç membrana erişmesine ve nihayetinde bakterileri öldürmesine izin veren membran boşluklarına neden olan dış membran dengesizleşmesine ve çıkıntılarına neden olur. Metabolik olarak inaktif hücrelerde, bağlanma iç membrana erişime izin vermek için yeterli değildir.
Bir yanıt yazın