YENİArtık Haberler makalelerini dinleyebilirsiniz!
ABD Gıda ve İlaç İdaresi, ileri meme kanseri için yeni bir tedaviyi onayladı.
Uyuşturucu üreticisi Eli Lilly, 25 Eylül'de, belirli hastalık tipleri olan yetişkinleri tedavi etmek için oral östrojen reseptörü antagonisti Inluriyo'nun onayını duyurdu.
Bu tipler arasında östrojen reseptörü pozitif (ER+), insan epidermal büyüme faktörü reseptörü 2-negatif (HER2–), ESR1 mutasyonlu ileri veya metastatik meme kanseri bulunur.
Kilo kaybı sadece bir hap olabilir, yeni ilaç çalışması önerir
Bir basın açıklamasına göre, günde bir kez hap, en az bir endokrin (hormon) tedavisi hattıdan sonra hastalık ilerlemesini görenler için de tasarlanmıştır.
Faz 3 EMBER-3 çalışmasında Inluriyo'nun endokrin tedaviye kıyasla kanser ilerlemesi veya ölüm riskini% 38 azalttığı bildirildi.
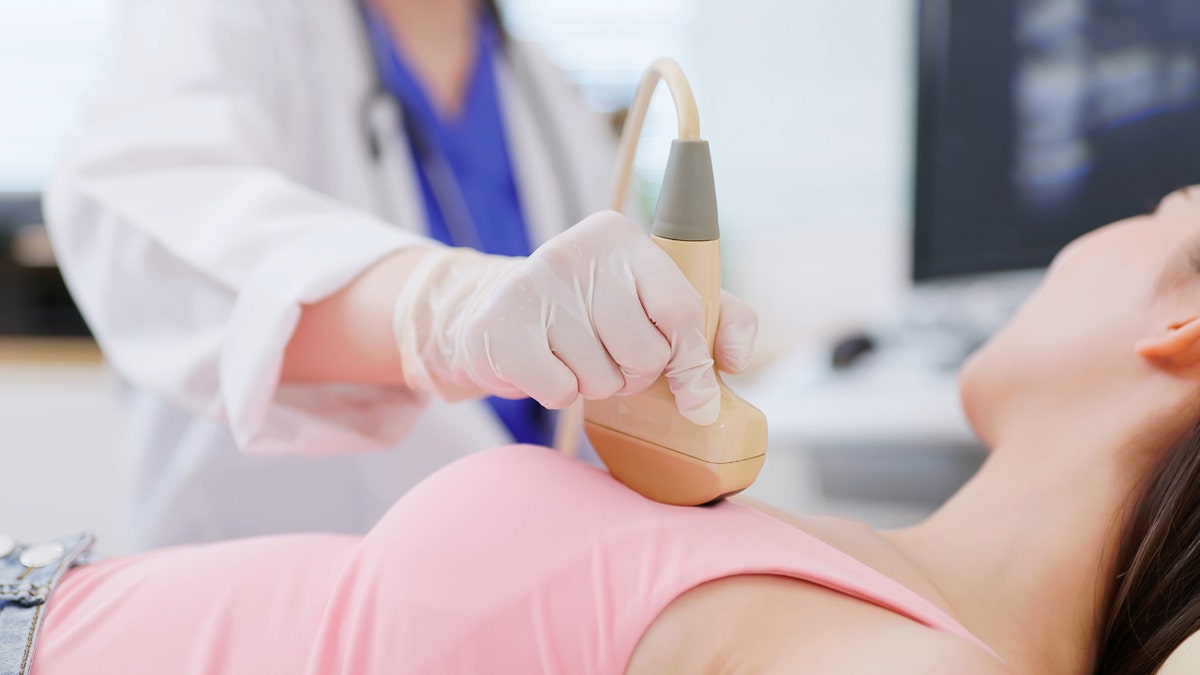
Uyuşturucu üreticisi Eli Lilly, 25 Eylül'de, belirli meme kanseri türlerine sahip yetişkinleri tedavi etmek için oral östrojen reseptörü antagonisti Inluriyo'nun onayını duyurdu. (Istock)
ESR1-mutasyonlu metastatik meme kanseri olan hastalarda, Fulvestrant veya Exemestan gibi diğer hormon tedavilerine kıyasla, 5½ aya karşı 3.8 aya göre ortalama sağkalım ile inluriyo ile progresyonsuz sağkalımda “önemli” bir iyileşme gördüler.
İşlev ve yan etkiler
Eli Lilly, bazı kanserler östrojen reseptörlerinin “aşırı aktif olmasına ve kanser büyümesini artırmasına” neden olabilecek mutasyonlar geliştirdi.
Inluriyo, hastalık ilerlemesini yavaşlatmaya yardımcı olan “bu reseptörlerin bozulmasını” bağlamak, engellemek ve kolaylaştırmak için çalışır.
Kanser aşısı, pankreas, kolorektal tümörlerin nüksünü önlemede umut vaat ediyor
“Bu, hormon tedavileri alan hastaların neredeyse yarısında bulunan, genellikle tedavi direncine katkıda bulunan bir mutasyon olan ESR1-mutasyonlu MBC hastaları için önemli bir ilerlemeyi temsil etmektedir.”
“Gösterilen etkinliği, tolere edilebilirlik profili ve oral uygulamasıyla bu tedavi, bu hasta popülasyonu için anlamlı bir alternatif tedavi seçeneği sunmaktadır.”
Bir zamanlar hapı, en az bir endokrin (hormon) tedavisinden sonra hastalık ilerlemesini görenler için de tasarlanmıştır. (Istock)
Inluriyo, doğmamış bir bebek için tehlikeli olabileceğine dair bir uyarı ile gelir, bu da hamile veya hamile kalabilecek kadınların onu almadan önce doktorlarıyla konuşmaları gerektiği anlamına gelir.
Faz 3 çalışması sırasında, yaygın yan etkiler “düşük dereceli” idi, ancak laboratuvar anormallikleri, kas -iskelet ağrısı, yorgunluk, bulantı, kabızlık, karın ağrısı, kolesterol ve trigliseritlerde bir azalma ve hemoglobin, kalsiyum, gezi, beyaz kan hücresi ve bazı enzimlerde bir azalma, çoğunlukla FDGE'de bulundu.
Diyerek şöyle devam etti: “Hastaların bilgili, bireyselleştirilmiş rehberlik almasını sağlamak çok önemlidir.”
Hastaların yaklaşık% 4.6'sı bu olumsuz olaylardan dolayı tedaviyi durdururken,% 2.4'ü dozlarını azalttı ve% 10'unda doz kesintileri vardı.
'Umutlu ama uyanık'
Indianapolis'teki Lilly Onkoloji Genel Müdür Yardımcısı ve Başkanı Jacob Van Naarden, bu terapinin “meme kanseri olan insanlar için sonuçları iyileştiren ve yenilikçi, tamamen oral tedavi yaklaşımlarını ilerletmeye yönelik önemli bir adımı temsil eden tedavilere olan bağlılığımızı yansıttığını” söyledi.
Haberler uygulamasını almak için buraya tıklayın
“Bu terapi, tedavi yolculuğunu meme kanseri ile yaşayanlar için daha yönetilebilir hale getirme potansiyeline sahiptir.”
Eli Lilly, Inluriyo'nun ER+, HER2-erken meme kanseri olan hastalar için devam eden Faz 3 Ember-4 çalışmasında artan nüks riskinde incelenmeye devam edeceğini paylaştı. Bu çalışma küresel olarak yaklaşık 8.000 hastayı kaydedecektir.
Şirkete göre Inluriyo'nun ABD'de “önümüzdeki haftalarda” bulunması bekleniyor.

“Bu terapi, tedavi yolculuğunu meme kanseri ile yaşayanlar için daha yönetilebilir hale getirme potansiyeline sahiptir.” (Istock)
New York'taki Memorial Sloan Kettering Kanser Merkezi'nde radyolog ve göğüs görüntüleme direktörü Haberler Medical katılımcısı Dr. Nicole Saphier, Haberler Digital ile yapılan bir röportajda uyuşturucu onayına tepki gösterdi.
Sağlık bültenimize kaydolmak için buraya tıklayın
“FDA, bu yeni ilacı onaylarken, Ember-3 denemesinde ilerleme veya ölüm riskinde% 38 azalma gösteren yeni, kanıta dayalı bir seçenekle birinci basamak tedavilere direnç geliştiren hastalara” dedi.
“Sadece bu sabah, bu ESR1 mutasyonu nedeniyle kanseri devam eden bir kadın gördüm ve bunun gibi atılımlar manzarayı değiştiriyor – daha seçici tedaviler sunuyor ve bir zamanlar umutsuz umut hisseden insanlara veriyor.”
Daha fazla sağlık makalesi için www.Haberler/health adresini ziyaret edin.
Saphier, ölümcül kardiyovasküler olaylar da dahil olmak üzere bu tedavi ile ilgili potansiyel güvenlik sorunları hakkında “uyanık kalmanın” ve hastaların bilgilendirilmiş, bireysel rehberlik almalarını sağladığını ekledi. “

Bir yanıt yazın